新通藥物謀求科創(chuàng)板IPO上市 擬募資12.79億元
- 資本邦
- 2021-12-08 16:22:42
12月6日,資本邦了解到,西安新通藥物研究股份有限公司(下稱“新通藥物”)沖刺科創(chuàng)板上市獲上交所受理,本次擬募資12.79億元。
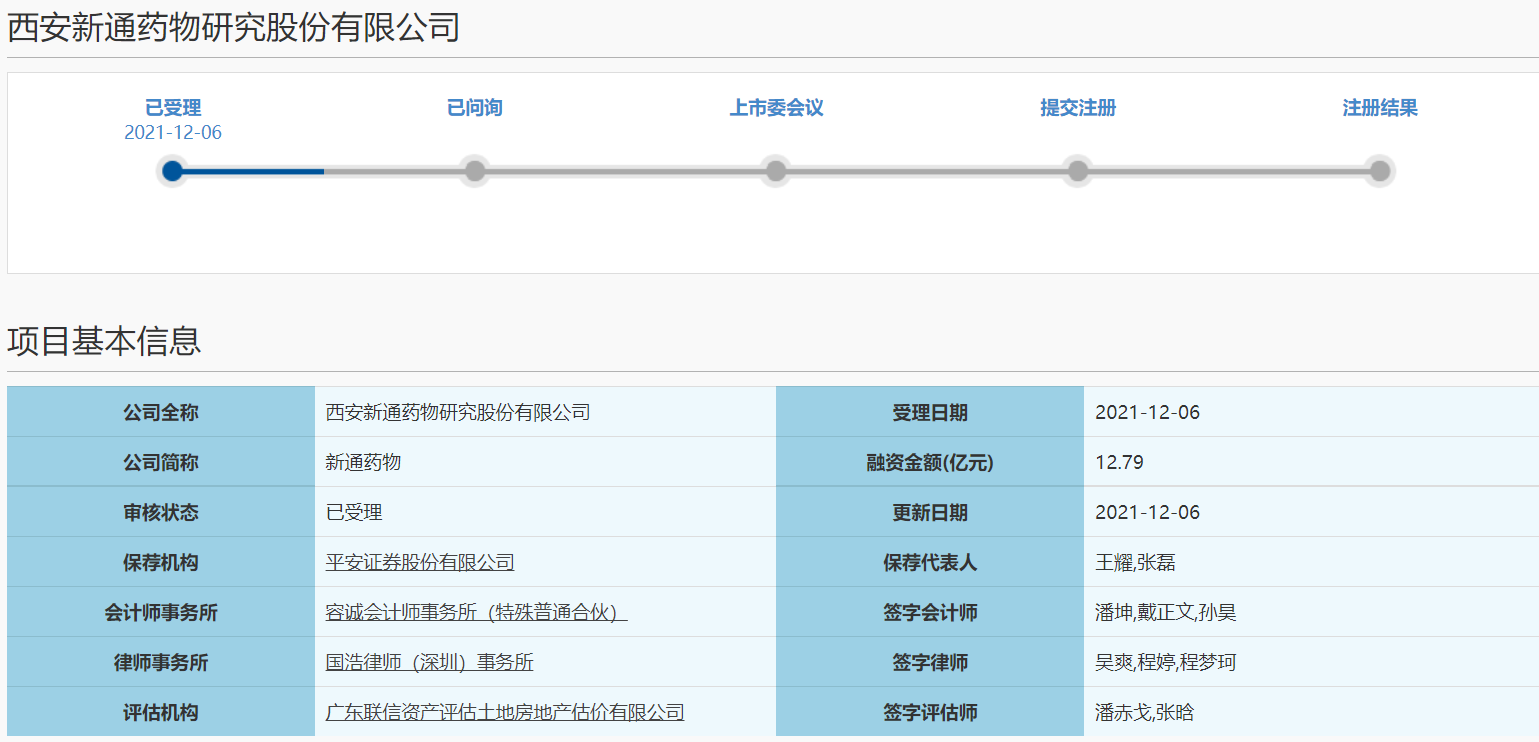
圖片來源:上交所官網(wǎng)
新通藥物是一家專注藥物研發(fā)超過二十年的高新技術(shù)企業(yè),現(xiàn)聚焦于慢性乙肝、肝癌、癲癇等重大疾病領(lǐng)域,致力于研發(fā)具有自主知識產(chǎn)權(quán)、安全有效、以臨床價值為導向的創(chuàng)新藥物。
財務數(shù)據(jù)顯示,公司2018年、2019年、2020年、2021年上半年營收分別為1,101.28萬元、1,387.90萬元、1,005.20萬元、0.21萬元;同期對應的凈利潤分別為-3,070.61萬元、-11,185.26萬元、-8,745.50萬元、-3,315.44萬元。
發(fā)行人符合并適用《上海證券交易所科創(chuàng)板股票發(fā)行上市審核規(guī)則》第二十二條規(guī)定的上市標準中的第(五)項標準:“預計市值不低于人民幣40億元,主要業(yè)務或產(chǎn)品需經(jīng)國家有關(guān)部門批準,市場空間大,目前已取得階段性成果。醫(yī)藥行業(yè)企業(yè)需至少有一項核心產(chǎn)品獲準開展二期臨床試驗,其他符合科創(chuàng)板定位的企業(yè)需具備明顯的技術(shù)優(yōu)勢并滿足相應條件。”
新通藥物稱,本次擬募資用于新藥研發(fā)項目、創(chuàng)新藥物產(chǎn)業(yè)化生產(chǎn)基地建設(shè)項目、補充流動資金項目。
截至本招股說明書簽署日,張登科直接持有公司50.60%股份,通過西安海金沙間接控制公司8.08%股份,張登科合計控制公司58.68%股份,為發(fā)行人的控股股東、實際控制人。
新通藥物坦言公司面臨以下風險:
(一)公司核心產(chǎn)品尚未上市銷售,公司尚未盈利并預期持續(xù)虧損
截至本招股說明書簽署日,公司核心產(chǎn)品仍處于研發(fā)階段,尚未開展商業(yè)化生產(chǎn)銷售,公司尚未盈利且存在累計未彌補虧損。報告期內(nèi),公司歸屬于母公司普通股股東的凈虧損分別為-3,070.61萬元、-11,185.26萬元、-8,745.50萬元和-3,315.44萬元,扣除非經(jīng)常性損益后歸屬于母公司普通股東的凈虧損分別為-4,967.22萬元、-4,273.74萬元、-9,842.04萬元和-4,030.19萬元。截至2021年6月末,公司未分配利潤為-10,467.81萬元。未來一段時間內(nèi),公司預期存在累計未彌補虧損并將持續(xù)虧損。
(二)公司預期未來需要較大規(guī)模的持續(xù)研發(fā)投入
報告期內(nèi),公司投入大量資金用于產(chǎn)品管線的臨床前研究、臨床試驗及新藥上市前準備。2018年、2019年、2020年及2021年1-6月,公司研發(fā)費用分別為4,339.49萬元、11,948.97萬元、8,874.23萬元和3,033.96萬元。截至本招股說明書簽署日,公司擁有9個在研項目,其中1個已提交上市許可申請,3個處于臨床試驗的不同階段,5個處于臨床前研發(fā)階段。公司未來仍需較大規(guī)模的持續(xù)研發(fā)投入,用于在研項目的臨床前研究、臨床試驗及新藥上市申請等研發(fā)活動。未來一段時間內(nèi),公司預期將持續(xù)虧損,累計未彌補虧損將持續(xù)擴大。
(三)公司無法保證取得新藥的上市批準,核心在研藥品上市存在不確定性
發(fā)行人核心在研產(chǎn)品CE-磷苯妥英鈉注射液已于2021年7月提交上市許可申請,目前在國家藥品審評中心(CDE)審評中,預計于2022年可獲得上市批準;發(fā)行人核心在研產(chǎn)品甲磺酸帕拉德福韋片預計于2023年提交上市許可申請。
由于新藥審評審批存在較大的不確定性,公司無法保證提交的新藥上市申請能夠取得監(jiān)管機構(gòu)的批準。如公司在研藥品的獲批時間較發(fā)行人預期有較大延遲,或無法就在研藥品獲得新藥上市批準,或該等批準包含重大限制,則將對公司的業(yè)務經(jīng)營造成重大不利影響,公司核心在研產(chǎn)品能否于預期時間內(nèi)順利獲得監(jiān)管機構(gòu)批準上市亦存在不確定性。
(四)公司無法保證未來幾年內(nèi)實現(xiàn)盈利,公司上市后亦可能面臨退市風險
公司未來幾年將存在持續(xù)大規(guī)模的研發(fā)投入,研發(fā)費用將持續(xù)處于較高水平,上市后未盈利狀態(tài)預計持續(xù)存在且累計未彌補虧損可能繼續(xù)擴大。
若公司核心產(chǎn)品的上市進程受到較大程度的延遲或無法獲得上市批準、獲批上市后商業(yè)化進展不達預期,自上市之日起第4個完整會計年度觸發(fā)《科創(chuàng)板股票上市規(guī)則》第12.4.2條的財務狀況,即經(jīng)審計扣除非經(jīng)常性損益前后的凈利潤(含被追溯重述)為負且營業(yè)收入(含被追溯重述)低于1億元,或經(jīng)審計的凈資產(chǎn)(含被追溯重述)為負,則可能導致公司觸發(fā)退市條件。
公司核心產(chǎn)品無法獲得上市批準,并且其他在研產(chǎn)品臨床試驗進展不及預期,公司可能觸發(fā)《科創(chuàng)板股票上市規(guī)則》第12.4.3條的規(guī)定,即公司的主要產(chǎn)品研發(fā)失敗或者未能取得藥品上市批準,且公司無其他業(yè)務或者產(chǎn)品符合《科創(chuàng)板股票上市規(guī)則》第2.1.2條第五項規(guī)定要求,則亦可能導致公司觸發(fā)退市條件。根據(jù)《科創(chuàng)板上市公司持續(xù)監(jiān)管辦法(試行)》,公司觸及終止上市標準的,股票直接終止上市,不再適用暫停上市、恢復上市、重新上市程序。
(五)營運資金不足的風險
在研藥物產(chǎn)生銷售收入前,公司需要在臨床前研究、臨床研究和市場推廣等諸多方面投入大量資金。報告期內(nèi),公司經(jīng)營活動產(chǎn)生的現(xiàn)金流量凈額分別為-2,324.79萬元、-6,102.57萬元、-7,677.05萬元及-2,691.20萬元。成功上市前,
公司營運資金依賴于外部融資,如經(jīng)營發(fā)展所需開支超過可獲得的外部融資,將會對公司的資金狀況造成壓力。如公司無法在未來一定期間內(nèi)取得盈利或籌措到足夠資金以維持營運支出,公司將被迫推遲、削減或取消公司的研發(fā)項目,影響在研藥品的商業(yè)化進度,從而對公司業(yè)務前景、財務狀況及經(jīng)營業(yè)績構(gòu)成重大不利影響。
(五)甲磺酸帕拉德福韋片、注射用MB07133、富馬酸海普諾福韋片、CE-磷苯妥英鈉注射液專利到期的風險
甲磺酸帕拉德福韋片、富馬酸海普諾福韋片的化合物結(jié)構(gòu)的中國專利已于2020年3月3日到期,注射用MB07133的化合物結(jié)構(gòu)的中國專利將于2023年10月31日到期,不排除化合物專利到期后,相關(guān)藥品被其他公司仿制的風險。
在上述各產(chǎn)品上市后,根據(jù)《中華人民共和國藥品管理法實施條例》對批準生產(chǎn)的新藥設(shè)置了最長5年的新藥監(jiān)測期規(guī)定,在這一期間,該制度將有效的阻止仿制藥的上市。不排除專利或藥品監(jiān)測期到期后市場上會出現(xiàn)甲磺酸帕拉德福韋片、注射用MB07133、富馬酸海普諾福韋片的仿制藥。仿制藥的上市將加劇市場競爭,或?qū)е鹿菊{(diào)低現(xiàn)有產(chǎn)品的價格。CE-磷苯妥英鈉注射液的藥品組合物專利將于2036年到期。作為一款化學藥三類藥物,CE-磷苯妥英鈉注射液不適用于“新藥監(jiān)測期”制度,不排除專利到期后市場上會出現(xiàn)CE-磷苯妥英鈉注射液的仿制藥。上述因素可能對公司的銷量及銷售價格產(chǎn)生不利影響。
(六)公司的在研產(chǎn)品基于專利授權(quán)的風險
公司部分核心在研項目的技術(shù)來源于合作方的授權(quán),自獲得相關(guān)授權(quán)許可以來,公司合作方均嚴格履行授權(quán)許可協(xié)議。報告期內(nèi),公司未與授權(quán)許可合作方發(fā)生過權(quán)屬爭議或其他法律糾紛。但未來如由于雙方在協(xié)議履行方面產(chǎn)生爭議,導致技術(shù)授權(quán)狀態(tài)發(fā)生變化,公司將可能面臨實際無法繼續(xù)在授權(quán)區(qū)域內(nèi)獨占使用相關(guān)技術(shù)的權(quán)利,或者繼續(xù)使用將會陷入法律爭議和糾紛的情形,進而造成公司的知識產(chǎn)權(quán)利益風險,并最終對公司創(chuàng)新藥物研發(fā)和后續(xù)注冊上市產(chǎn)生不利影響。(陳蒙蒙)
關(guān)鍵詞: 新通藥物 科創(chuàng)板IPO 業(yè)績虧損 營運資金不足
鄧長昌:盡快對我省科技特派員制度進行系統(tǒng)總結(jié)
- 黃月珍:推進綜合改革打造臺灣同胞“第二生活圈”
- 李家榮:優(yōu)化創(chuàng)新生態(tài)掀起新一輪民營經(jīng)濟發(fā)展熱潮
- 黃玲:全方位構(gòu)建幸福養(yǎng)老服務體系在創(chuàng)造高品質(zhì)生活上實現(xiàn)更大突破
- 李金算:加快構(gòu)建政府公共數(shù)據(jù)服務體系打造“便利福建”
- 春節(jié)期間遼寧對道路交通安全形勢進行分析研判 提供安全順暢的交通環(huán)境
- 福建省一批民生項目建設(shè)取得顯著成效
- 福建省十三屆人大六次會議在福州開幕
- 去年福建全省地區(qū)生產(chǎn)總值48810億 今年預期增長6.5%
- 福建省新型冠狀病毒肺炎疫情情況
- 兩部門發(fā)布《意見》:要求各部采取針對性舉2022-01-24
- 鄧長昌:盡快對我省科技特派員制度進行系統(tǒng)2022-01-24
- 黃月珍:推進綜合改革打造臺灣同胞“第二生2022-01-24
- 李家榮:優(yōu)化創(chuàng)新生態(tài)掀起新一輪民營經(jīng)濟發(fā)2022-01-24
- 黃玲:全方位構(gòu)建幸福養(yǎng)老服務體系在創(chuàng)造高2022-01-24
- 李金算:加快構(gòu)建政府公共數(shù)據(jù)服務體系打造2022-01-24
- 住建部在全國推進住房公積金“跨省通辦” 2022-01-24
- 數(shù)據(jù)顯示:2021年全年城鎮(zhèn)新增就業(yè)1269萬人2022-01-24
- 云南安寧打破農(nóng)民職業(yè)發(fā)展“天花板” 開展2022-01-24
- 2021年遼寧省糧食生產(chǎn)形勢喜人 糧食總產(chǎn)量2022-01-24
- 春節(jié)期間遼寧對道路交通安全形勢進行分析研2022-01-24
- 遼寧海城市確保全年簽約億元以上項目超過652022-01-24
- 遼寧盤錦公布12件民生實事 推進高質(zhì)量發(fā)展2022-01-24
- “有夢 有為”周末青年志愿行動在李滄舉行2022-01-24
- 聽·見 | 動畫師變身面塑傳承人,這個802022-01-24
- 26名群眾代表青島占倆!高二學生成省政協(xié)旁2022-01-24
- 追蹤丨全民接力,傳來好消息!即墨失聯(lián)3天2022-01-23
- 立案查處!青島昌明置業(yè)有限公司森林公園項2022-01-23
- 半島驗房丨膠州億陽金都馨城毛坯房墻面銹點2022-01-23
- “樂動市南”!逛街時與藝術(shù)不期而遇,“浮2022-01-23
- 人間煙火氣!逛吃、選年貨、置辦新衣服……2022-01-23
- 浮山灣夜靜悄悄2022-01-23
- 民俗大拜年,非遺專家亮絕活!2022年山東省2022-01-23
- 風雨無阻!嶗山區(qū)實驗學校小學部的足球隊員2022-01-23
- 市北區(qū)探索服務賦能新路徑 營造企業(yè)發(fā)展好2022-01-23
- 市北區(qū)聚焦中醫(yī)藥長遠建設(shè),產(chǎn)生“雙驅(qū)動”2022-01-23
- 福建省一批民生項目建設(shè)取得顯著成效2022-01-23
- 福建省十三屆人大六次會議在福州開幕2022-01-23
- 去年福建全省地區(qū)生產(chǎn)總值48810億 今年預2022-01-23
- 福建省新型冠狀病毒肺炎疫情情況2022-01-23